- 「電池」:化学的エネルギー(酸化還元反応)を電気的エネルギー(電子の流れ)に変換する装置
- 元素の「陰性」と「陽性」
- 陰性:電子を引き付ける性質
- 陽性:電子を放出する性質


- 負極:電子を放出する極(陽性の強い元素)
- 正極:電子を受け取る極(陰性の強い元素)
- ボルタ電池:(-)Zn|H2SO4aq|Cu(+)
負極:Zn→Zn2++2e-
正極:2H++2e-→H2
金属のイオン化傾向(陽性の強さの順位)K Ca Na Mg Al Zn Fe Ni Sn Pb H2 Cu Hg Ag Pt Au
- 燃料電池(リン酸を用いるもの):(-)H2|H3PO4aq|O2(+)
負極:H2→2H++2e-
正極:O2+4e-+4H+→2H2O
燃料電池(水酸化カリウムを用いるもの):(-)H2|KOHaq|O2(+)
負極:H2→2H++2e-
正極:O2+4e-+2H2O→4OH-
この世で一番陰性が強い元素はフッ素(F)、その次が酸素(O)。
非金属元素の中で水素(H)は、最も陰性が弱い。 - 「太陽電池」:太陽光のエネルギー(光エネルギー)を原子が受け取ると、電子を放出する(光電効果)を直接利用(化学反応ではない)
- 元素の「陰性」と「陽性」
- 「電気分解」:電気的エネルギーを加えて化学反応(酸化還元反応)を行わせること
- 陽極:電池の正極とつながった極
(電子を奪われる) - 陰極:電池の負極とつながった極
(電子を受け取る)
- 陽極:電池の正極とつながった極
- 重力による位置エネルギー:mgh
質量m、基準面からの高さhに比例する(比例係数を「重力加速度」gという) - 運動エネルギー:
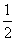 mv2
mv2
質量m、速さvの2乗、に比例する
- 「外部」との他のエネルギーのやり取りがないときは、i,iiの合計は一定である
- 「外部」の例:動摩擦力による「仕事」
- 動摩擦力μ'mg(質量mに比例)
- 「仕事」=「力」×「距離」
| [例]塩化ナトリウム水溶液(白金電極) | ||
| 陽極反応 | 陰極反応 | |
| 2Cl- → Cl2 + 2e- | 2H2O + 2e- → H2 + 2OH- | |
| [1]希塩酸(白金電極) | ||
| 陽極反応 | 陰極反応 | |
|
|
|
|
| [2]希硫酸(白金電極) | ||
| 陽極反応 | 陰極反応 | |
|
|
|
|
| [3]水酸化ナトリウム水溶液(白金電極) | ||
| 陽極反応 | 陰極反応 | |
|
|
|
|
| [4]硫酸銅水溶液(白金電極) | ||
| 陽極反応 | 陰極反応 | |
|
|
|
|
| [5]硫酸銅水溶液(銅電極) | ||
| 陽極反応 | 陰極反応 | |
|
|
|
|
| [6]硝酸銀水溶液(白金電極) | ||
| 陽極反応 | 陰極反応 | |
|
|
|
|
| [7]硝酸銀水溶液(銀電極) | ||
| 陽極反応 | 陰極反応 | |
|
|
|
|